新一代人工膜肺:PDMS微流体氧合器
人工肺作为ECMO的核心部件,其材料发展经历了三代:第一代为固体硅胶膜,相容性好、血浆渗漏少,但排气困难、预充量大、跨膜压差大;随后第二代以PP聚丙烯微孔中空纤维为代表的膜肺解决了排气困难的问题,但微孔结构会导致血浆渗漏的可能性较高,寿命较短;第三代PMP中空纤维膜,是目前正在广泛应用的材料。其结合了一代和二代膜材料的优点,具有较薄的致密层,可以有效防止血浆泄漏,使用寿命大大延长。不过由于中空纤维膜尺寸与结构上的限制,由其制成的膜式氧合器与人体生理肺的功能仍相差甚远。
因此,PDMS微流体氧合器成为了新一代人工膜肺的发展方向。基于微流体技术并采用更高性能膜材料—聚二甲基硅氧烷(PDMS)制成的氧合器能最大程度接近人体肺功能。
微流体技术是生物医学应用领域的新兴工具。它的出现为解决ECMO的一些关键性问题提供了新的思路。因为微流体能够塑造比中空纤维膜氧合器更薄的气体转移膜和更浅的血液通道,能大大提高气体交换能力;并且由于其特征尺寸和通道设计与生理情况较为相似,可以更好地模拟生理气体转移过程中血液流经肺部小血管的方式;此外,微流体较小的表面积和体积能减小设备尺寸;与人肺相似的血流网络可改善生物相容性。
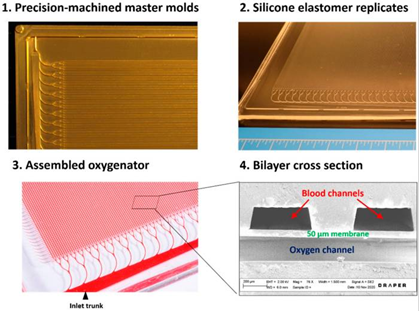
微流体氧合器组件的图像
微流体氧合器装置由三层组成,一层为氧气层,连接着携氧通道;另一层为血管层,由载血通道网络组成,两层之间被极薄的PDMS膜隔开;整体呈现出一种三明治结构。血管网络层经过精心设计以最小化血液上的剪切力,降低对流经血液的破坏。

微流体氧合器的制作工艺
此外,为了能更好地复制和模拟人肺的 3D 微体系结构和微环境、呼吸运动以及主要生理功能,一些生物混合型肺辅助模型也应运而生。这种结合了微流体和器官芯片技术的模型,同样是在PDMS膜的基础上构造微通道,上通道为肺泡上皮细胞排列的肺泡通道,下通道为肺血管内皮排列的血管通道,通过机械拉伸形成肺泡-毛细血管屏障的膜来模拟生长期的呼吸模式。当该模型实际应用到膜式氧合器上时,就可利用逆流血液和气流,对血液进行氧合。

内皮细胞包被的PDMS膜氧合器模型
目前,已有较多研究证明PDMS微流体氧合器在短期内能保持气体交换的稳定,未来的试验将通过更长期、更大规模的测试验证该装置的适用性,为ECMO新一代膜肺的开发和临床使用铺平道路。
参考文献:
1.Hellmann A, Klein S, Hesselmann F, et al. EndOxy: Mid-term stability and shear stress resistance of endothelial cells on PDMS gas exchange membranes. Artif Organs. 2020;44(10):E419-E433.
2.Santos J, Vedula EM, Lai W, et al. Toward Development of a Higher Flow Rate Hemocompatible 3.Biomimetic Microfluidic Blood Oxygenator. Micromachines (Basel). 2021;12(8):888.
Potkay JA. The promise of microfluidic artificial lungs. Lab Chip. 2014;14(21):4122-4138.

